

了解蒸汽
H2O的三相分別為冰、水和蒸汽。
分子是靠電荷力(氫鍵)緊密地結合在一起,分子運動的活躍程度決定了物質的相。像其它物質一樣,在某個特定溫度和壓力下H2O的三相達到平衡狀態而共存,這就是H2O的三相點。H2O的三相點,也就是冰、水和蒸汽三相共存點,是溫度273.16 K和絕對壓力0.006112 bar。此時的壓力非常接近絕對真空,如果在此溫度下壓力進一步下降,冰就會直接升華為蒸汽。
冰
的分子以點陣形式有序地排列,它們僅能在其平衡位置附近振動。振動的幅度不會超過分子直徑。 熱量的持續增加會導致分子振動加劇,并最終相互脫離,于是固體開始融化為液態(無論何種壓力下總是在0℃時開始融化)。冰融化時雖然發生了相變,但冰的溫度并不上升,此時吸收的熱量稱為熔解熱。相變現象是可逆的,當水結冰時會有同樣多的熱量釋放到周圍環境中。
大多數物質由固態變為液態的時候,其密度將會下降。然而,H2O是一個例外,當冰融化成水的時候,它的密度會增加,這就是為什么冰會浮于水上和水結冰后體積變大的原因。
水
在液態下,分子可以自由移動,但是由于相互之間的吸引力作用,其移動距離仍然小于一個分子的間距,分子之間的碰撞經常發生。不斷增加的熱量增加了分子運動和碰撞,并把液體的溫度提高到汽化的溫度,這個階段吸收的熱量稱為水的液體焓或顯熱。通常,我們把0℃水的焓定義為零。 在大氣壓 (0barg)下,水在100℃時沸騰,把1kg水從0℃加熱到100℃需要419kJ的熱量,由此可以 推導出水的比熱容Cp是4.19kJ/(kg?℃)。
蒸汽
當水的溫度上升到沸騰狀態時,一些分子得到了足夠的動能,具有了足夠的速度,這樣就可以在落回液體中之前從液體表面逸出。繼續加熱使分子運動進一步加劇,大量的分子具有離開液面的動能。當水被加熱到沸點時,氣泡從水中逸出并在表面爆裂。
由于蒸汽的分子之間距離要大的多,蒸汽的密度比水低的多,所以蒸汽會存在于水的表面以上的空間。 當離開液體表面的分子比那些重新進入液面的分子多的時候,水會自由蒸發。這時,它已經達到了它的沸點或飽和溫度。如果壓力保持不變,增加更多的熱量不會使水溫上升,但會使水變成飽和蒸汽。同一系統下飽和水的溫度與飽和蒸汽溫度相同,但單位質量蒸汽中的含熱量要比飽和水大得多。
在大氣壓力下,飽和溫度是100℃。壓力上升,飽和水的溫度也隨著上升,焓值也會提高。飽和蒸汽壓力和溫度之間的關系曲線如下:
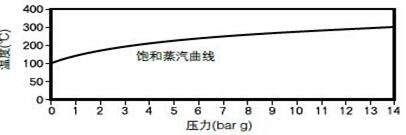
在該曲線上,水和蒸汽可以在任何壓力下共存,飽和曲線以上是過熱蒸汽。飽和溫度以上的溫度稱為蒸汽的過熱度。飽和曲線下的水稱為過冷水。